醫療器械CA證書是干什么用的?醫療器械CA證書申領資料
2019年5月31日,國家藥監局發布了《關于實施醫療器械注冊電子申報的公告(2019年第46號)》,從2019年6月24日正式實施電子申報,從11月1日起提交國家局的注冊資料都需要按照電子申報目錄
來源:醫療器械注冊代辦 發布日期:2024-01-19 閱讀量:次
GCP證書,全名叫“藥物臨床試驗質量管理規范”證書(雖然名字帶“藥物”,但醫療器械臨床試驗同樣適用這個規范),是證明一個人接受過GCP培訓并且通過考核的憑證。現在很多搞臨床試驗的同行,不管是藥企的、CRO公司的(合同研究組織)、還是醫院的研究者、護士、臨床協調員(CRC)、臨床監察員(CRA),都在琢磨要不要考一個。這證書到底有多大分量?考了是不是真管用?值不值得花時間去拿?這是不少人心里犯嘀咕的事。

說GCP證書的“含金量”,得看它是不是硬性要求。在咱們國家,干臨床試驗這行,特別是關鍵崗位,GCP證書基本是必備的敲門磚。國家藥監局(NMPA)發布的《醫療器械臨床試驗質量管理規范》(2022年第28號公告)和《藥物臨床試驗質量管理規范》(2020年第57號公告)都寫得明明白白:參與臨床試驗的人員,特別是主要研究者和參與試驗的醫生、護士這些,必須都經過GCP培訓。 醫院(臨床試驗機構)要承接項目,倫理委員會要審項目,藥監局來檢查,頭一件事就是查關鍵人員有沒有GCP培訓證明(也就是證書)。你沒這個證,醫院可能不讓你當主要研究者(PI),公司可能不讓你負責監察項目(CRA)或者協調工作(CRC)。所以,從“合規上崗”這個硬杠杠來看,GCP證書的含金量非常高——沒它,你連參與核心工作的資格都沒有。
但是,光有證就夠了嗎?肯定不夠。證書只能證明你學過、考過了GCP的基本規則和要求,知道啥該做、啥不該做。它不能自動證明你真會干、能干好臨床試驗。臨床試驗是個實操性極強的活,從方案設計、病人招募、知情同意、數據記錄、安全性報告到現場監查、問題處理,每一步都需要經驗、判斷力和責任心。一個剛拿證的新手CRA,和一個干了十年、處理過各種復雜情況的老CRA,那水平肯定不一樣。所以,業內真正看重的,是“證書”背后的實際經驗和能力。證書是基礎門檻,是入場券,但進去之后能走多遠、爬多高,還得看真本事。當然,對于招聘方來說,有證至少說明這人懂規矩、有基礎,招進來能更快上手。

| 角度看含金量 | 含金量體現 | 需要注意的點 |
|---|---|---|
| 法規合規性 | 非常高:國家法規強制要求關鍵崗位人員必須持有。無證無法擔任主要研究者(PI)、無法在合規的臨床試驗機構承擔核心工作。藥監局檢查必查項。 | 證書是上崗的“硬通行證”。 |
| 求職應聘 | 高:招聘CRA、CRC、臨床試驗項目經理、研究護士等崗位時,GCP證書通常是基本要求或優先條件。有證比沒證機會多。 | 是簡歷篩選的“硬指標”之一。 |
| 實際工作能力 | 基礎證明:僅證明持有人知曉GCP基本原則和要求,不等于具備熟練的實操技能、問題解決能力和經驗。 | “有證”不代表“能干”,經驗積累和實戰能力更重要。 |
| 行業認可度 | 普遍認可:是臨床試驗從業人員專業性的基礎標識,業內普遍認可其必要性。 | 屬于行業“標配”。 |
| 證書來源差異 | 有區別:國家藥監局高級研修學院、中國藥學會等權威機構頒發的證書認可度最高;部分線上速成班頒發的證書可能含金量打折扣。 | 認準權威發證機構。 |
總結
GCP證書的含金量,在“合規上崗”和“求職敲門”這兩點上,非常高,甚至可以說是必需的。沒它,你連參與臨床試驗核心工作的門都進不去,招聘方第一關就可能刷掉你。但是,它最大的價值是證明你“懂規矩”,是基礎門檻。真正在行業里站穩腳跟、做出成績,光靠證書遠遠不夠,關鍵還得看你的實踐經驗、解決問題的能力、責任心這些真本事。所以結論是:干這行,GCP證書該考必須考,這是硬要求;但考過了也別覺得萬事大吉,持續學習、積累經驗才是提升你個人“含金量”的根本。

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫療科技有限公司專注于醫療器械產品政策與法規規事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創新辦理服務。

2019年5月31日,國家藥監局發布了《關于實施醫療器械注冊電子申報的公告(2019年第46號)》,從2019年6月24日正式實施電子申報,從11月1日起提交國家局的注冊資料都需要按照電子申報目錄

歐盟自由銷售證明是指歐盟國家主管當局出具的自由銷售證書,全稱為Certificate of Free Sale或Free Sales Certificate,簡稱CFS或FSC。本文重點講解企業申請歐盟自由銷售證書的條件和自由銷售證

GMP、GLP和GCP是什么?GMP(GOOD MANUFACTURING PRACTICE)良好生產規范:世界衛生組織將GMP定義為指導食物、藥品、醫療產品生產和質量管理的法規。GMP要求制藥、食品等生產企業應具備良好的

目前國際通行的GCP是ICH-GCP,我國執行的是國家食品藥品監督管理局(SFDA)頒布的中國GCP。中國現行GCP是2020年頒布,與ICH-GCP相比,具有中國特色。中國GCP是以ICH-GCP為藍本,結合我國的實

GCP證書會過期嗎?針對這個問題,特地查詢了目前我國所有的臨床現行法律法規,都沒有發現GCP證書有效期的規定。對于GCP證書的更新問題,業內有傳言五年一延續的說法,下面一起來

1.試驗用醫療器械的研制應當符合適用的醫療器械______相關要求。A.質量管理體系B.風險管理C.經營管理體系D.使用管理體系

GCP證書有用嗎?有用有用非常有用,GCP證書是臨床行業的的準入門檻,也就是說,想要從事臨床試驗,必須要持有GCP證書。GCP證書適用人員GCP不但適用于即將或已經取

ICH-GCP是藥品國際注冊中共認的GCP。ICH-GCP列出的13條基本原則是GCP的科學性和倫理性原則的集中體現,是ICH-GCP的精華所在。隨著我國藥品審評審批制度改革的深入推進,我國GCP與ICH-GCP全面接
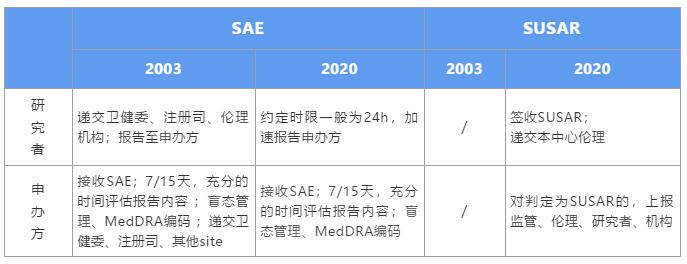
新版GCP對于申辦方的影響是全方位的,就SAE個例報告處理方面,強化了申辦方的主體責任,細化了申辦方對SAE的管理流程。在此,我們詳細解讀,在新規之下,該如何高效、合規的處理

說真的,最近除了口罩,還是口罩。現在朋友圈問最多的,就是口罩能不能出口啊,需要什么資質和證明啊……昨天有人轉發一文章給我,說口罩被扣的,因為CE認證不被國外海關認可,
行業資訊
知識分享
八年
醫療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
