干貨|臨床SSU工作內(nèi)容和具體工作流程
SSU是Study Start Up的縮寫,從最初的項目準備,到啟動訪視(Site Initiation Visit)之前所有的準備工作,對整個臨床研究項目的啟動非常關鍵。負責這個關鍵階段工作的部門人員,就叫做SS


注冊備案 · 臨床試驗 · 體系建立輔導 · 分類界定 · 申請創(chuàng)新
來源:醫(yī)療器械注冊代辦 發(fā)布日期:2023-10-10 閱讀量:次
?
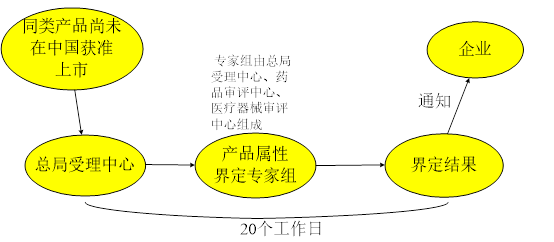
本文源自《關于調(diào)整藥械組合產(chǎn)品屬性界定有關事項的通告(2019年第28號)》附件:藥械組合產(chǎn)品屬性界定工作流程,如果您對自家新研發(fā)產(chǎn)品無法判定是醫(yī)療器械?是藥物?還是藥械組合?您可以依據(jù)以下方式申請進行藥械組合產(chǎn)品屬性界定。

申請人通過中國食品藥品檢定研究院(國家藥品監(jiān)督管理局醫(yī)療器械標準管理中心)網(wǎng)站(網(wǎng)址:http://www.nifdc.org.cn/)進入“醫(yī)療器械標準管理中心”二級網(wǎng)站(網(wǎng)址:https://www.nifdc.org.cn/nifdc/bshff/ylqxbzhgl/index.html),點擊進入“藥械組合產(chǎn)品屬性界定信息系統(tǒng)”,填寫《藥械組合產(chǎn)品屬性界定申請表》,并上傳其他申請資料。
(一)藥械組合產(chǎn)品屬性界定申請表
(二)支持性材料
1.產(chǎn)品描述
產(chǎn)品的名稱、組成成分(所含成分劑量)、組合方式、預期用途、使用時與患者接觸部位/接觸時間、產(chǎn)品示意圖、實物照片等。
2.作用機制
組合產(chǎn)品及各組成成分的作用機制,主要及次要作用方式,并提供相關的支持和驗證性資料。
3.擬采用的使用說明書(或用戶手冊等)
4.組合產(chǎn)品各組成成分來源
5.申請人屬性界定意見及論證資料
組合產(chǎn)品實現(xiàn)預期目的的首要作用方式、確定依據(jù)和支持性試驗資料及文獻資料,對組合產(chǎn)品中發(fā)揮、部分發(fā)揮和不發(fā)揮主要作用的組分進行系統(tǒng)論證并提供支持性資料。
6.相關產(chǎn)品的描述及監(jiān)管情況
明確藥械組合產(chǎn)品中藥品或組分按藥品管理及其佐證資料。如已有相似或相關的產(chǎn)品在境內(nèi)或境外上市,簡要介紹該產(chǎn)品結構、組成(含量)、預期用途等基本情況、管理屬性和類別及支持性資料。對于境外產(chǎn)品屬性界定申請,應同時提交該組合產(chǎn)品在其當?shù)厣鲜械馁Y料。
7.其他與產(chǎn)品屬性確定有關的資料
在線打印《藥械組合產(chǎn)品屬性界定申請表》并簽字簽章,掃描后連同其他申請資料一并按要求上傳。所有申請資料應當使用中文。根據(jù)外文資料翻譯的,應當同時提供原文。
申請人登陸“藥械組合產(chǎn)品屬性界定信息系統(tǒng)”即可查詢申請狀態(tài)和結果。
網(wǎng)址:http://app.nifdc.org.cn/biaogzx/login.do?formAction=login&yxzh=yxzh

站點聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點,也不代表本網(wǎng)對其真實性負責。圖片版權歸原作者所有,如有侵權請聯(lián)系我們,我們立刻刪除。如有關于作品內(nèi)容、版權或其它問題請于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應并做相關處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務服務,提供產(chǎn)品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創(chuàng)新辦理服務。

SSU是Study Start Up的縮寫,從最初的項目準備,到啟動訪視(Site Initiation Visit)之前所有的準備工作,對整個臨床研究項目的啟動非常關鍵。負責這個關鍵階段工作的部門人員,就叫做SS

初次申請消字號備案,總會遇到磕磕絆絆的問題,常見的有申請流程、申請資料、申請周期等問題,本文將對申請消字號產(chǎn)品流程及費用簡單概述,對即將進入消毒產(chǎn)品行業(yè)的企業(yè)做一

大多數(shù)CRO公司在臨床試驗現(xiàn)場啟動會(SIV)上,常由CRA主導。作為一名有上進心的CRA必須清楚的了解到臨床試驗現(xiàn)場啟動考察的流程,再分享一些本人在啟動會考察的細節(jié),請看下文。

關中心訪視(Close Out Visits,簡稱COV),想必大家都聽說過。作為臨床試驗最后一個階段,COV也是非常重要的一個環(huán)節(jié),今天和大家分享一下作為監(jiān)查員在COV時應該做哪些工作。什么時候

2019年5月31日,國家藥監(jiān)局發(fā)布了《關于實施醫(yī)療器械注冊電子申報的公告(2019年第46號)》,從2019年6月24日正式實施電子申報,從11月1日起提交國家局的注冊資料都需要按照電子申報目錄

目前,臨床研究注冊的要求是,前瞻性隨機對照研究必須在研究開始前注冊,觀察性研究目前尚無統(tǒng)一要求,但有需要注冊的趨勢(脊柱外科前瞻性的研究不注冊,文章一般很難發(fā)表,
眾所周知,醫(yī)療器械分為三類,一類采用備案制,二三類采用注冊制管理,等級越高,管理越嚴格。一類醫(yī)療器械都是免臨床的,因此備案工作比較簡單不繁瑣。而二三類醫(yī)療器械除免臨床產(chǎn)品

根據(jù)《醫(yī)療器械監(jiān)督管理條例》(國務院令第650號),第三類醫(yī)療器械注冊時需要提交產(chǎn)品的檢測報告,并且注冊申請資料中的產(chǎn)品檢測報告應當由具有承檢資格的醫(yī)療器械檢驗機構出具

歐盟自由銷售證明是指歐盟國家主管當局出具的自由銷售證書,全稱為Certificate of Free Sale或Free Sales Certificate,簡稱CFS或FSC。本文重點講解企業(yè)申請歐盟自由銷售證書的條件和自由銷售證

我們都知道,一個醫(yī)療器械產(chǎn)品想要上市銷售除了辦理醫(yī)療器械生產(chǎn)許可證外,還需要辦理醫(yī)療器械注冊證,而三類醫(yī)療器械產(chǎn)品又屬于風險級別最高,管控級別也最嚴,那么三類醫(yī)療器械產(chǎn)品
行業(yè)資訊
?
?
?
?
?
?
知識分享
八年
醫(yī)療器械服務經(jīng)驗
聯(lián)系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊臨床第三方平臺
