山東省醫療器械工藝用水現場檢查指南(魯藥監械〔2021〕35號)
為規范醫療器械現場檢查,提升檢查員現場檢查能力,指導檢查員對醫療器械生產企業工藝用水控制情況的檢查,提高企業工藝用水質量安全保證水平,依據《醫療器械監督管理條例》
來源:醫療器械注冊代辦 發布日期:2023-10-10 閱讀量:次
?
瓊藥監注〔2020〕16號
海南博鰲樂城國際醫療旅游先行區各相關醫療機構:
《海南博鰲樂城國際醫療旅游先行區醫療機構制劑調劑使用管理暫行辦法》已經3月24日海南博鰲樂城國際醫療旅游先行區領導小組會議審議通過,現印發給你們,請遵照執行。
附件:海南博鰲樂城國際醫療旅游先行區醫療機構制劑調劑使用管理暫行辦法(瓊藥監注〔2020〕16號).doc
海南省藥品監督管理局
2020年4月3日
(此件主動公開)
第一條 為加強海南博鰲樂城國際醫療旅游先行區(以下簡稱先行區)醫療機構制劑調劑使用管理,根據《中華人民共和國藥品管理法》《醫療機構制劑注冊管理辦法》和《關于支持建設博鰲樂城國際醫療旅游先行區的實施方案》,結合先行區醫療機構的實際情況,制定本辦法。
第二條 本辦法所指的醫療機構制劑為根據《醫療機構制劑注冊管理辦法》取得制劑批準文號或根據《關于對醫療機構應用傳統工藝配制中藥制劑實施備案管理的公告》取得醫療機構傳統中藥制劑備案資格的藥品。
第三條 先行區內醫療機構申請醫療機構制劑調劑使用以及相關監督管理工作,適用本辦法。
第四條 醫療機構制劑調劑使用的調出方應具有《醫療機構制劑許可證》,具備開展制劑全項檢驗所必需的藥學技術人員、設施和檢驗儀器等;配制制劑所需的場地、設施設備及生產技術人員、質量管理等必須符合《醫療機構制劑配制管理規范》要求,配制規模應滿足本機構及調出制劑數量的需要,提出申請調劑的品種近二年內未出現制劑質量事故,無藥品監督管理部門抽樣檢驗不合格情況。
第五條 申請醫療機構制劑調劑使用,應當由調入方醫療機構填寫《醫療機構制劑調劑使用申請表》,向海南省藥品監督管理局提出申請,并提供以下證明性文件:
(一)制劑調出和調入方的《醫療機構執業許可證》副本復印件;
(二)調出方《醫療機構制劑許可證》復印件;
(三)擬調劑品種的制劑批準證明文件復印件;
(四)擬調劑的理由、用途、范圍、數量和使用期限;制劑調劑雙方簽署的合同原件;
(五) 擬調劑品種的質量標準,說明書、包裝和標簽樣稿;
(六)調出方出具的該批次制劑品種的自檢報告書;
(七)跨省的制劑調劑,需經調出方所在地省藥品監督管理局同意。
第六條 調出方的義務和責任:
(一)提供《醫療機構制劑許可證》及制劑批準文件;
(二)調出的制劑經檢驗合格;
(三)對調出制劑的質量負責;
(四)調出的制劑不能超出《醫療機構制劑調劑使用批件》所載明批準的期限、數量和使用范圍。
第七條 調入方的義務和責任:
(一)嚴格按照說明書使用醫療機構制劑;
(二)調入的制劑不能超出《醫療機構制劑調劑使用批件》所載明批準的期限、數量和使用范圍;
(三)調入的制劑應當按要求貯存;
(四)調入的制劑不得流入市場銷售;
(五)調入制劑只能在本醫療機構內憑醫師的處方使用,并與《醫療機構執業許可證》所載明的診療范圍相適應。
第八條 海南省藥品監督管理局收到調劑申請10個工作日內作出審批決定,符合要求的,批準調劑,發給《醫療機構制劑調劑使用批件》;不符合要求的,不予調劑,書面通知申請人并說明理由,同時告知申請人享有依法申請行政復議或者提起行政訴訟的權利。
第九條 須經國家藥品監督管理局批準調劑使用的調劑申請,應當由取得制劑批準文號的醫療機構向所在地省、自治區、直轄市藥品監督管理局提出申請,說明使用理由、期限、數量和范圍,經審查同意后,由使用單位將審查意見和相關資料一并報送海南省藥品監督管理局審核同意后,報國家藥品監督管理局審批。
第十條 申請制劑調劑的醫療機構有下列情形之一的,海南省藥品監督管理局不予受理或者不予批準:
(一)宣傳或變相宣傳制劑療效的;
(二)申請調劑制劑品種近兩年內抽驗出現不合格的;
(三)提供虛假申報資料、證明文件的;
(四)不按要求上報制劑不良反應的。
第十一條 醫療機構制劑不得在市場上銷售或者變相銷售,不得發布醫療機構制劑廣告。
第十二條 對提供虛假證明文件、申報資料或者采取其他欺騙手段申請制劑調劑使用的,海南省藥品監督管理局一年內不受理其申請;已取得調劑使用批件的,撤銷其批件。
第十三條 調劑使用制劑的醫療機構應當注意觀察制劑不良反應,并按照《藥品不良反應報告和監測管理辦法》的要求報告和處理。
第十四條 醫療機構制劑在市場上銷售或者變相銷售、或未經批準,擅自將配制的制劑調劑給其他醫療機構使用的、以及擅自使用其他醫療機構配制的制劑的,依照《藥品管理法》等法律法規的規定給予處罰。
第十五條 本辦法由海南省藥品監督管理局負責解釋。
第十六條 本辦法自印發之日起施行。

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫療科技有限公司專注于醫療器械產品政策與法規規事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創新辦理服務。
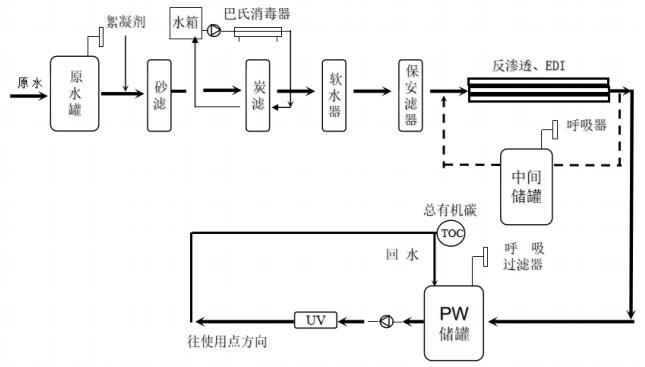
為規范醫療器械現場檢查,提升檢查員現場檢查能力,指導檢查員對醫療器械生產企業工藝用水控制情況的檢查,提高企業工藝用水質量安全保證水平,依據《醫療器械監督管理條例》
《化妝品生產經營監督管理辦法》已經2021年7月26日市場監管總局第12次局務會議通過,現予公布,自2022年1月1日起施行。
《海南博鰲樂城國際醫療旅游先行區臨床急需進口藥品帶離先行區使用管理暫行辦法》已經3月24日海南博鰲樂城國際醫療旅游先行區領導小組會議審議通過,現印發給你們,請遵照執行

為深入貫徹落實中共中央辦公廳、國務院辦公廳印發的《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),按照國家藥品監督管理局《關于擴大醫療器械

為規范醫療器械注冊人跨區域委托生產的監督管理,推進長江三角洲區域醫療器械跨區域監管,根據《中共中央辦公廳國務院辦公廳關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》《

關于發布醫療器械質量管理體系年度自查報告編寫指南的通告(2022年第13號)發布時間:2022-03-24為加強醫療器械生產監管,保障醫療器械安全有效,根據《醫

國家藥監局關于發布免于進行臨床評價醫療器械目錄的通告(2025年第19號)發布時間:2025-05-13為做好醫療器械注冊管理工作,根據《醫療器械注冊與備案管理

為加強醫療器械生產監督管理,規范醫療器械生產質量管理,根據《醫療器械監督管理條例》(國務院令650號)、《醫療器械生產監督管理辦法》(國家食品藥品監督管理總局令第7號)

附件:醫療器械監督管理條例(2025年修訂版).doc醫療器械監督管理條例(2000年1月4日中華人民共和國國務院令第276號公布 2014年2月12日國務院第

附件:重組膠原蛋白創面敷料注冊審查指導原則(2023年第16號).doc重組膠原蛋白創面敷料注冊審查指導原則本指導原則旨在指導注冊申請人準備及撰寫重組膠原蛋白創
行業資訊
知識分享
八年
醫療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
